湘雅二医院陈翔宇团队为深部肿瘤治疗提供新思路
来源:湘雅二医院 点击次数:次 发布时间:2025年08月22日 作者:兰婕 刘梅桃
本网讯 近日,中南大学湘雅二医院陈翔宇团队在国际学术期刊《今日材料物理》(Materials Today Physics)发表原创研究“一种新型癌症放射光动力治疗方式:伽玛刀联合铜半胱胺纳米颗粒介导的光动力疗法对肝癌的协同治疗研究(A novel modality of radiation photodynamic therapy for cancer: the combination therapy of gamma knife and Cu-Cy nanoparticle mediated photodynamic effect on liver cancer)”,为深部肿瘤治疗提供新模式。湘雅二医院陈翔宇主任医师与西交利物浦大学陈伟教授为共同通讯作者,湘雅二医院2020级硕士生刘梅桃与博士生王天明为共同第一作者,湘雅医院神经外科刘渊渊为重要参与作者,中南大学湘雅二医院为论文第一署名单位。
在临床肿瘤治疗中,伽玛刀是一种广泛应用于颅内肿瘤和脑血管病变的高精度放射外科设备。它能将上百束伽玛射线从不同角度汇聚于肿瘤靶点,精准打击、无创介入,常被誉为“不开刀的手术刀”。近年来,随着技术发展,伽玛刀也被逐步探索应用于神经系统以外的实体瘤治疗。研究显示,由于肝癌对放疗的敏感性较高,这为伽玛刀在该领域的拓展提供了可能。其高剂量精准照射可迅速缩小肿瘤体积,缓解癌性疼痛和阻塞性黄疸等症状,尤其适用于晚期或无法手术的患者,显著改善生活质量。但伽玛刀的应用也面临许多挑战:多数肝癌患者合并肝硬化,放疗可能加剧肝功能损伤,导致肝衰风险上升。同时,针对直径较大、分布多灶或已转移的病灶,单一局部放疗往往难以奏效。因此,当前研究趋势强调伽玛刀与其他治疗方式的联合应用,以兼顾疗效、安全性与系统治疗能力。
在此背景下,光动力治疗(PDT)成为一种值得关注的补充手段。PDT通过“光+光敏剂”协同作用,在肿瘤局部产生活性氧(ROS)杀伤癌细胞,并可激活免疫反应。它具备高选择性、低毒性、微创等优势,已在皮肤癌、食管癌等浅表肿瘤中广泛应用。然而,传统PDT多依赖激光或红外光作为激发源,这类光在人体组织中的穿透力有限,难以作用于肝癌等深部实体瘤。为突破限制,研究团队创新性地提出以伽玛射线作为光动力激发源的思路,构建深部可达的放射-PDT协同治疗模式。
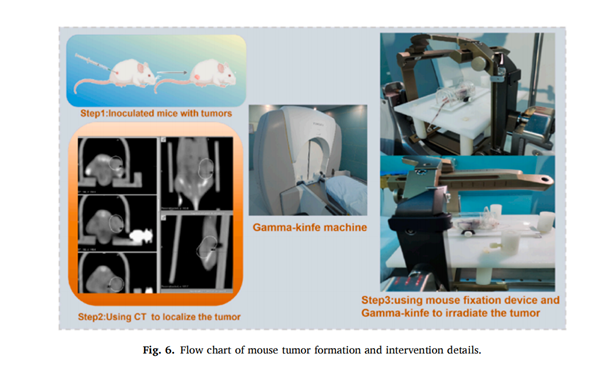
相比已有数万篇文献研究的红外激发光动力,全球尚无关于“伽玛射线激发光动力”的系统性生物学研究报道。研究团队在无先例可参考的前提下,开展跨学科合作,整合放射医学、纳米材料、光化学等多学科力量,在历经三年探索、多轮实验后首次证实:伽玛射线可高效激活铜半胱胺(Cu-Cy)纳米光敏剂,促使其在深部肿瘤微环境中产生活性氧(ROS),并显著抑制肿瘤生长。这一突破使“伽玛射线驱动的PDT治疗”从假设走向现实,填补了深部PDT治疗领域的关键空白。
研究团队首次实验证实Cu-Cy在伽马射线作用下可发生剂量依赖性的ROS生成反应,揭示了该模式在物理机制层面的可行性。在细胞与动物水平,该组合策略可显著抑制多种肝癌细胞增殖与迁移,可诱导细胞坏死,使肿瘤明显缩小且无明显毒性作用,且显示出优异的靶向性与生物相容性,具备极强的临床转化潜力。另外,该治疗模式在肿瘤微环境响应方面亦展现出独特优势:在弱酸性环境下ROS生成效率进一步增强,提示其具备“肿瘤特异性激活”机制,有望克服传统疗法对肿瘤异质性的适配障碍。
本研究在不改变现有放疗系统框架与光敏剂材料结构的基础上,通过激发方式的原创性重构,实现了对传统PDT治疗深度与靶向性的双重突破,代表着深部肿瘤精准治疗路径的一次“范式转变”。其“可穿透、可聚焦、可激发”的特征,使其兼具高度创新性、临床可及性与工程可实施性,在肝癌等深部实体瘤治疗中展现出“一体两效”的协同治疗潜力。此次研究的成功,标志着团队在高能射线激发光动力治疗领域实现了从“理论构想”到“实践证明”的关键跨越,也为未来深部肿瘤治疗提供了具有原创性的高效技术方案。
(一审:何美琴 二审:邓皓迪 三审:李殷 )









 分享:
分享: