中南大学赵岳涛课题组开发新型仿生光热免疫刺激纳米药物
来源:生命科学学院 点击次数:次 发布时间:2024年05月09日 作者:胡艺俏
本网讯 近日,中南大学生命科学学院赵岳涛课题组在国际期刊《纳米生物学技术杂志》(Journal of Nanobiotechnology)在线发表题为“仿生纳米药物阻断CD73抑制腺苷并与光热刺激系统增强抗肿瘤免疫响应(Biomimetic nanodrug blocks CD73 to inhibit adenosine and boosts antitumor immune response synergically with photothermal stimulation)”的研究论文。该研究成功设计并合成了一种新型仿生光热免疫刺激纳米药物,通过光热效应和抑制CD73蛋白协同促进抗肿瘤免疫响应,有效抑制肿瘤生长,并具有良好的安全性,在肿瘤的光免疫治疗方向显示出良好的应用潜力。
肿瘤免疫治疗面临响应率较低的问题,由三磷酸腺苷(ATP)经细胞表面蛋白CD73分解生成的腺苷是一种重要的免疫抑制因子,对免疫细胞的抗肿瘤活性产生强抑制效应,通过抑制CD73阻断腺苷的产生,可以促进抗肿瘤免疫反应。光热治疗(PTT)是通过光热效应杀伤肿瘤细胞,同时诱导肿瘤细胞的免疫原性细胞死亡(ICD),引发死亡肿瘤细胞释放损伤相关分子模式(DAMPs),可以有效地促进免疫响应。基于上述原理,赵岳涛课题组将CD73抑制剂5′-(α,β-亚甲基)二磷酸-腺苷(AMPCP)和光热剂黑磷量子点(BPQDs)封装在壳聚糖纳米凝胶中,并在壳聚糖纳米凝胶表面包覆了肿瘤靶向性适体AS1411修饰的红细胞膜(EM),成功构建了具有腺苷调控功能的仿生光热免疫纳米药物AptEM@CBA。通过AS1411引导下的主动靶向和EM赋予的长血液循环时间,促进了纳米药物在肿瘤位点的富集。光热治疗可促进免疫激活,同时,通过释放AMPCP阻断CD73的腺苷生成途径,减轻腺苷对树突状细胞的功能损伤,并抑制调节性T细胞(Tregs)、髓源性抑制细胞(MDSC)、M2型肿瘤相关巨噬细胞(TAMs)的功能,从而协同刺激T细胞活性。CD73阻断与PTT的结合,不仅能抑制原发性植入肿瘤的生长,还激发了有效的抗肿瘤免疫响应,抑制远端肿瘤的生长。
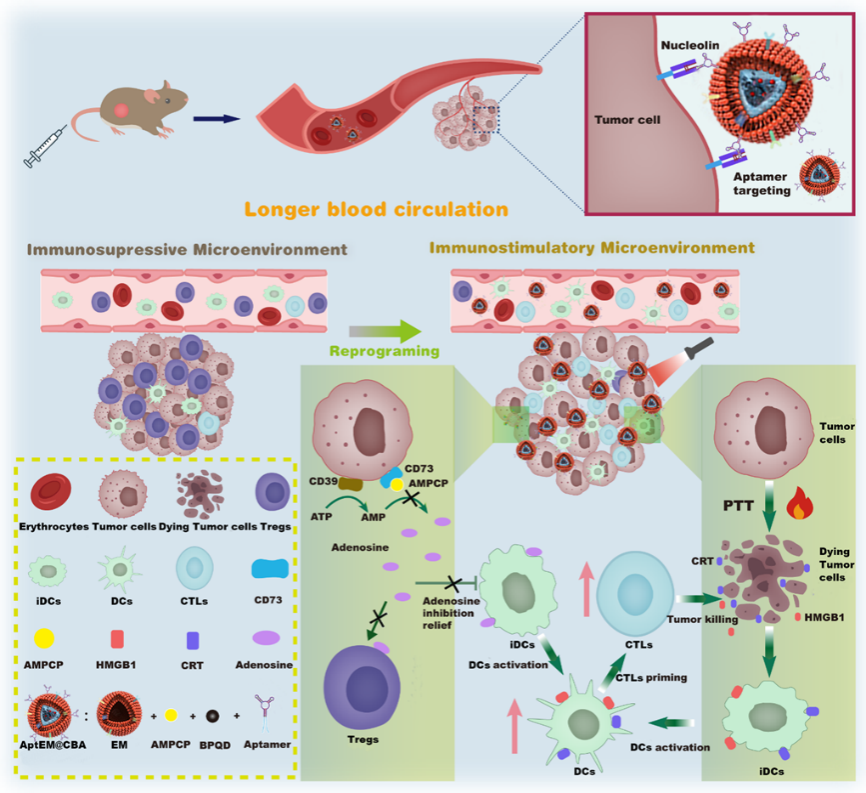
仿生光热免疫纳米药物AptEM@CBA激活抗肿瘤免疫响应的模式图
以上工作受到国家自然科学基金、湖南省自然科学优秀青年基金、湖南省教育厅优秀青年基金等项目的支持,中南大学生命科学学院为第一作者单位,中南大学生命科学学院生物化学与分子生物学系硕士研究生李坦和张星宇为并列第一作者,赵岳涛为论文通讯作者。
(一审:张贝 二审:王轩 三审:李殷)









 分享:
分享: