中南大学李发祥团队联合发文揭秘细菌与噬菌体“暗战”的新机制
来源:生命科学学院 点击次数:次 发布时间:2024年08月14日 作者:胡艺俏
本网讯 近日,中南大学生命科学学院李发祥教授团队联合西湖大学史竹兵研究员、湖南师范大学杨荣教授科研团队在国际知名期刊《自然-通讯》(Nature Communications)发表题为《NAD+水解酶DSR2被噬菌体蛋白激活与抑制的结构基础》 (The structural basis of the activation and inhibition of DSR2 NADase by phage proteins) 的原创性学术论文成果。李发祥、史竹兵和杨荣为该论文的共同通讯作者,中南大学生命科学学院2022级硕士研究生王瑞文和西湖大学生命科学学院博士研究生许奇为论文的共同第一作者,中南大学生命科学学院为该论文的第一作者和第一通讯作者单位。
在自然界中,细菌与噬菌体之间的斗争从未停歇。为了抵御噬菌体的侵袭, 细菌、古菌等微生物已经进化出了多种多样的免疫防御系统,包括限制修饰(RM)系统、CRISPR-Cas 系统和顿挫感染(abortive infection)系统等。其中,顿挫感染系统通过诱导被噬菌体感染细菌的自杀,阻止噬菌体的传播,从而保护细菌群体的生存。DSR 系统就是这类顿挫感染免疫系统的一种,该系统的核心因子是一种具备降解NAD+活性(NADase)的DSR2蛋白。DSR2是一种含有Sir2结构域的蛋白,通过水解NAD+诱导细胞死亡来保护细菌免受噬菌体感染。DSR2的酶活性可以被噬菌体SPR的尾管蛋白(TTP)激活,而被SPbeta噬菌体编码的DSAD1蛋白抑制,使噬菌体能逃避宿主防御。然而,DSR2被噬菌体激活和抑制分子机制一直未知。
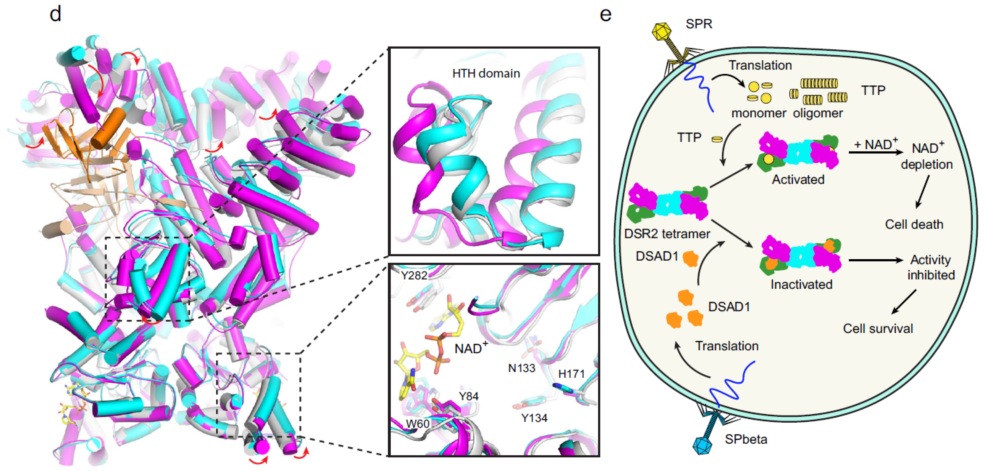
DSAD1和TTP竞争性的结合 DSR2调控其NAD+水解酶活性示意图
本研究利用冷冻电镜技术解析了DSR2单体、DSR2-TTP-NAD+复合物和DSR2-DSAD1复合物的三维结构。结果显示,DSR2以“头对头”四聚体的形式组装,该四聚体由Sir2结构域介导。DSR2的C末端螺旋区域构成四个底物结合腔,呈开放和闭合两种构象。两个TTP分子结合到四个C末端腔中的两个,诱导Sir2结构域发生构象变化从而激活DSR2。此外,DSAD1能与激活剂竞争性结合到DSR2的C末端腔,有效抑制其酶活性。该研究阐明了DSR2介导的抗噬菌体防御系统以及DSAD1介导的噬菌体免疫逃避的分子机制。这不仅有助于我们深入理解细菌免疫系统的工作原理,也为针对细菌和噬菌体之间的“军备竞赛”寻找新的突破口提供了重要依据。通过理解这些复杂的分子相互作用,科学家们可以设计出更有效的策略来对抗多药耐药细菌,为未来的抗菌治疗开辟新的道路。
本研究得到国家自然科学基金、湖南省“荷尖”人才项目和湖南省自然科学基金等项目支持。
(一审:韩艳 二审:余学飞 三审:唐潇珺)









 分享:
分享: