湘雅医院曾珊/韩莹/申竑团队发表肿瘤领域系列研究成果
来源:湘雅医院 点击次数:次 发布时间:2025年04月15日 作者:吴丽丹 汤宇
本网讯 近日,中南大学湘雅医院肿瘤科曾珊、韩莹、申竑教授团队在国际知名期刊《自噬》(Autophagy)上发表了题为“HMBOX1通过促进HACE1诱导的ATG5泛素化降解逆转自噬介导的结直肠癌5-氟尿嘧啶耐药(HMBOX1 reverses autophagy mediated 5-fluorouracil resistance through promoting HACE1-induced ubiquitination and degradation of ATG5 in colorectal cancer)”的原创研究性论文。该研究揭示了转录因子HMBOX1通过调控E3泛素连接酶HACE1,促进ATG5泛素化降解,从而抑制自噬,增强结直肠癌细胞对5-FU的敏感性,为克服治疗耐药提供了潜在新靶点。中南大学湘雅医院为第一单位和唯一通讯单位,曾珊教授、韩莹副教授、申竑教授为共同通讯作者,2022级博士研究生高燕为第一作者。
结直肠癌是全球范围内发病率和致死率居高不下的重大公共健康问题。5-FU作为当前治疗方案中的核心药物之一,在临床中发挥重要作用。然而,药物耐受性的产生严重影响了治疗效果,成为当前研究领域亟待突破的瓶颈。本研究首次系统揭示了转录因子HMBOX1在调控自噬活性及影响结直肠癌对5-FU敏感性中的关键作用。研究发现, HMBOX1通过上调E3泛素连接酶HACE1的转录活性,促进其对自噬关键蛋白ATG5进行K63位点的泛素化修饰,从而驱动ATG5的蛋白酶体降解,最终抑制过度自噬,提升细胞对药物的敏感性。临床队列分析进一步验证了“HMBOX1–HACE1–ATG5”轴在结直肠癌药物反应性调控中的重要作用。
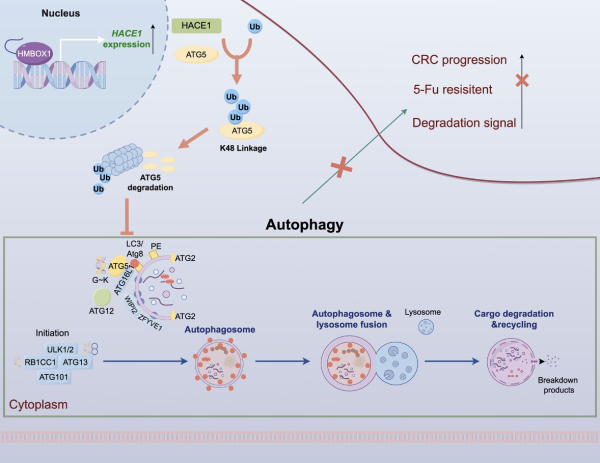
HMBOX1-HACE1-ATG5轴的关键调控作用机制图
这一发现不仅为结直肠癌耐药机制提供了全新视角,也为靶向自噬调控开辟了新的治疗策略方向。HMBOX1的表达水平有望成为预测患者药物反应性的重要生物标志物,而靶向激活HMBOX1或HACE1的干预手段,或可作为未来增强治疗效果、改善患者预后的潜在突破口。
(一审:赵云逸 二审:邓皓迪 三审:李殷)









 分享:
分享: